大会注册费用:
1.大会展区参观合作交流和品牌路演区:免费注册报名
2.大会论坛: 注册费2600元(含论坛门票、午餐券、会刊),2024年3月31日前注册,优惠价2000元。以下任意一种方式即可免费领取价值2600元的大会论坛门票:
(1)报名后即可预约机构和发布项目,完成10家参展机构预约;
(2)报名后就在报名链接右下角发布中心调研项目;
(3)邀请三人参会(报名后可再登录报名链接,点击查看报名信息,拉至末尾备注处填写推荐参会的单位和姓名)
(4)大会海报发朋友圈30个点赞。
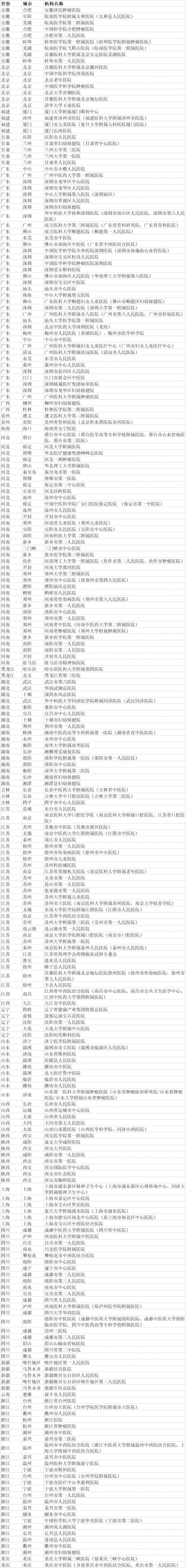
参展参会机构:
大会邀请400+参展参会机构和1500+申办方/CRO及第三方专业供应商等企业参展参会,目前已有四川大学华西医院、中国医学科学院肿瘤医院、四川省人民医院、兰州大学第一医院、兰州大学第二医院、上海交通大学医学院附属新华医院、北京地坛医院、广州中医药大学第一附属医院、四川省中医院、重庆市中医院、吉林省中医院、广州市妇女儿童医疗中心、河南省儿童医院、湖南省妇幼保健院、苏州市立医院、浙江省肿瘤医院、河南省肿瘤医院、西南医科大学附属医院、河南省传染病医院、西安市胸科医院、宜宾市第二人民医院、浙江省台州医院、皖南医学院弋矶山医院、新疆人民医院、甘肃省人民医院、山西省人民医院、山西白求恩医院、吉林大学第三医院、深圳市第二人民医院、浙江医院、惠州市中心人民医院、北京大学首钢医院、北京西苑医院、北京潞河医院等机构。
大会嘉宾:
国家药品监督管理局药品审评中心相关领导
中国医药质量管理协会及其CRO分会相关领导
田少雷(国家药监局核查中心原学术委员会副主任委员、处长)
魏万宏:(国家卫生健康委员会医院管理研究所特聘研究员)
孙瑞华(药审中心统计学审评专家、核查中心临床数据核查专家)
郑莉(四川省医师协会药物临床试验研究者分会会长)
60+医疗机构GCP分管院领导
BIOBAY相关领导
研发企业相关领导
参会人群:
1.临床试验机构 400+
GCP分管院领导、机构办负责人、研究者等;
2.申办方和CRO及其他临床研究供应商 1500+
企业负责人、中高层领导、临床运营总监/负责人/经理、PM、SSU负责人、KA、机构合作负责人、上市后项目负责人、医学、BD、QA、CRA、SMO SSU负责人、采购/供应商管理、市场负责人等。
大会论坛:
第一天 上午
开幕式
中国医药质量管理协会领导致辞、CRO分会领导致辞临床试验高质量监管和质量时代发展论坛
1、质量强国建设纲要解读(中国航空综合研究所中心副主任 倪超 教授)
2、新法规时代对药物临床试验机构的监督检查(国家药监局核查中心原学术委员会副主任委员 田少雷 处长)
3、管理工具在医疗机构质量管理中的应用(国家卫生健康委员会医院管理研究所特聘研究员 魏万宏)
4、《临床试验数据管理核查要点》团体标准解读国家药监局药审中心统计学审评专家、核查中心临床数据核查专家 孙瑞华)
第一天 下午
论坛一
新未来-中国临床研究多方合作发展与展望
1、新机遇,新挑战,齐奋进
(江苏恒瑞医药股份有限公司 火泽功 总监)
2、协同创新-CRO与临床试验机构合作关系探讨(博济医药 夏其奎 首席运营官)
3、临床试验院企合作的实践与展望(四川大学华西医院 郑莉主任)
4、PI职责下的高效入组和高质量执行(哈尔滨医科大学附属第四医院成志锋主任)圆桌讨论:中国临床研究发展的新机遇思考,新的合作关系期待新未来的畅想。
论坛二
新活力-医疗机构临床研究高质量发展暨GCP院长论坛
1、提升医疗机构临床试验水平,助力生物医药产业发展(苏州市立医院 孙茂才 副院长)
2、机遇与挑战:新形势下临床研究机构的发展(兰州大学第一医院 孟文勃 副院长)
3、以GCP为抓手,促进临床研究高质量发展(西南医科大学附属医院 万居易 常务副院长)
圆桌讨论:医企合作高峰对话
第二天 上午
论坛三
新布局-中国临床研究国际化发展高峰论坛
1、1CH框架下的质量保证(鼎晖思创总经理 高志刚)
2、加入全球产业链背景下的临床试验实施(远大医药临床运营高级总监 游丽芬)
3、GlobalCRO的管理与驱动(鑫康合生物临床开发副总裁 尤建国博士)
4、FDA与EMA核查经验与思考(浙江省肿瘤医院徐伟珍主任)圆桌讨论:中国生物医药产业出海合作和临床运营实施的挑战
论坛四:新质效-临床试验提质增效论坛
1、精细管理:Biotech临床项目管理模式探讨(南京艾美斐生物医药科技有限公司 高云临床运营总监)
2、临床试验中,SMO如何与各合作方配合提质增效(上海药明津石医药科技有限公司 李维霞高级临床研究总监)
3、国际多中心临床研究的高效管理(康龙临床副总裁 张海)
圆桌讨论:如何合力最优化提质增效?
第二天 下午
论坛五:新伙伴-临床试验泛供应链助力高质高效创新发展论坛
1、DCT生态共建与发展(泰格医药VP俞皎皎)
2、样本量:投入与风险的博弈(静远医药生物统计总监宫晓)
3、安全性事件管理跨部门协作(静远医药药物警戒总监陈文娜)
4、结合司法实践处理临床试验损害赔偿(北京君都律师所宋胜云律师)
5、从保险视角处理临床试验不良事件损害赔偿(上海五新保险 刘亚卿总监)
6、圆桌讨论:供应商管理风险及各方如何合作助力临床试验高质高效实施?
品牌路演:
GCP机构运营管理经验交流和GCP机构路演
1、深耕十三载 焕发新生态(宜宾市第二人民医院 何庆玲)
2、呵护生命 精业成医(核工业四一六医院 邵继春)
3、铁“骨”柔情,“麻”到不行(西安市红会医院 黄静、任安珺
4、临床研究助力专科医院高质量发展(郑州市第六人民医院赵玲5、扬帆前行,未来可期(襄阳市中心医院 徐少勇)
6、在竞争中求发展(新乡市第一人民医院 王志阳)
7、优秀的细节把控是临床试验的成功关键–案例分享(成都中医药大学附属医院(四川省中医院)南峰)
8、“向阳而生,逐光前行(中国医学科学院肿瘤医院深圳医院(深圳市肿瘤医院)秦燕)
9、横扫困扰 为你剖析大兴GCP高质服务(西安大兴医院 王莹)
10、科真伦善,逐鹿中原(濮阳油田总医院 于法明)
11、临研有道,出声显影(西安医学院第一附属医院 王莉)
12、稳重求进,步步为营(延安大学咸阳医院 白晓东
13、科学仁爱,长江之畔,横跨136年的弋矶山医院诚邀天下(皖南医学院弋矶山医院(皖南医学院第一附属医院)贾元威)
14、四川省人民医院药物临床试验机构优势介绍(四川省人民医院 杨孟昌)
15、创新治疗,神经内科临床试验引领前行(南阳市第二人民医院 王明)
16、推进临床试验工作 助力医院高质量发展(郑州市中心医院 何勐
17、”质量为先,效率同行 — 探索临床试验的最佳实践”(重庆市中医院 黄彦)
18、临床试验高质量管理探索:(中国医学科学院肿瘤医院 房虹)
19、早期临床试验高质量设计和实施的基本考量(北京地坛医院 胡朝英)
20、从核查角度浅淡临床试验质量管理(首都医科大学北京潞河医院 梁欣
21、探索与实践:研究型医院建设中的IT研究管理与实践重庆市中医院 黄彦)
22、金赛药业公司及产品管线简介(长春金赛药业有限责任公司李华刚)
23、浅谈核医学科建设(北京夸克侠科技有限公司 赵娜)
24、弯道超车:生物样本库在构建研究型医院与转化医学中的应用(诺擎生物科技(上海)有限公司 杨宇)
25、临床试验用药品智能管理方案(深圳市瑞意博医疗设备有限公司 陈苏静)
26、智慧临床研究平台赋能临床研究效率与质量提升长沙通诺信息科技有限责任公司 陈贝)
27、受试者补偿发放创新服务平台一受试者补偿与权益保护解决方案提供者(上海祎添医药科技开发有限公司 赵明远)
28、临床试验信息化管理增强机构运营能力 提高临床试验质量和效率(杭州揽萃医药科技有限公司 金晶)
29、上海首嘉公司简介(上海首嘉医学临床有限公司 余辈)
30、半导体高频超声影像项目介绍(珂纳医疗科技(苏州)有限公司蒋宁宁
31、伴随诊断整体解决方案领导者(迈杰转化医学研究(苏州)有限公司张亚飞)
32、穿透血脑屏障的药物开发(苏州韬略生物科技股份有限公司 张大为)持续更新中..
圆桌讨论:与机构合作的愉快和痛点及期待?
大会同期举办:
1.中国医药质量管理协会分支机构工作会议(G馆1楼)
2.GCP院长·GCP发展经验交流闭门会(2024年4月18号下午姑苏学院)
3.全临床试验全程项目实施风险与质量管理能力提升培训班(G馆1楼两天)
4.臻尚精品临床试验高级项目管理课程培训班(G馆1楼两天)

微信搜索公众号【苏州本地生活】关注后在对话框回复:
【景区预约】:园林、古镇等景区预约入口
【医保】:医保余额查询、家庭共济申请等
【公积金】:公积金贷款、提取、还款申请指南
【赏花】:苏州春季赏花推荐(梅花、樱花、桃花等)
【落户】:目前落户苏州(积分、人才引进、投靠)申请指南
【社区】:苏州各大社区联系方式
【积分】:2023年积分落户、入学、入医申请指南,测一测自己有多少积分
【学区】苏州各区域学区查询

 微信扫一扫
微信扫一扫 
